UNIDAD 4: La presión y formas de energia

Intercambio entre calor y trabajo
Es un concepto fundamental en la termodinámica, que describe cómo la energía puede transferirse entre un sistema y su entorno. El calor y el trabajo son dos formas en las que la energía puede fluir, pero se diferencian en cómo se transfieren y cómo afectan al sistema.
Energía Interna
La energía interna es la energía total contenida dentro de un sistema termodinámico debido a la interacción de sus partículas, como moléculas, átomos o iones.
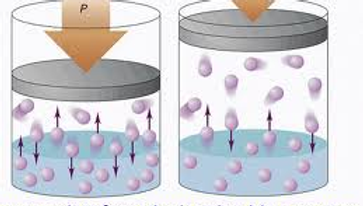
Primer principio de la termodinámica
También conocido como la ley de conservación de la energía, establece que la energía total de un sistema aislado se conserva. Es decir, la energía no se puede crear ni destruir, solo se puede transformar de una forma a otra.

La variación de energía interna de un sistema es igual a la suma del calor, Q, y el trabajo, W, intercambiados con el exterior.
Este video nos va a ayudar a entender mucho mejor la Primera ley de la termodinámica.
PARA VOLVER AL INICIO PULSA AQUI
Segundo principio de la termodinámica
La segunda ley de la termodinámica establece que la entropía (una medida del desorden o la dispersión de la energía) de un sistema aislado tiende a aumentar con el tiempo. En términos más simples, los procesos naturales siempre ocurren en una dirección que aumenta la entropía, es decir, la energía se dispersa de una forma menos organizada.

Con la ayuda del siguiente video vamos a tener mas claro como actúa la segunda ley de la termodinámica
